LA COMISIÓN EUROPEA,
Visto el Reglamento (CE) n.o 853/2004 del Parlamento Europeo y del Consejo, de 29 de abril de 2004, por el que se establecen normas específicas de higiene de los alimentos de origen animal (1), y en particular su artículo 7, apartado 2, letra a),
Visto el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo, de 9 de marzo de 2016, relativo a las enfermedades transmisibles de los animales y por el que se modifican o derogan algunos actos en materia de sanidad animal (Legislación sobre sanidad animal) (2), y en particular su artículo 238, apartado 3 y su artículo 239, apartado 3.
Visto el Reglamento (UE) 2017/625 del Parlamento Europeo y del Consejo, de 15 de marzo de 2017, relativo a los controles y otras actividades oficiales realizados para garantizar la aplicación de la legislación sobre alimentos y piensos, y de las normas sobre salud y bienestar de los animales, sanidad vegetal y productos fitosanitarios, y por el que se modifican los Reglamentos (CE) n.o 999/2001, (CE) n.o 396/2005, (CE) n.o 1069/2009, (CE) n.o 1107/2009, (UE) n.o 1151/2012, (UE) n.o 652/2014, (UE) 2016/429 y (UE) 2016/2031 del Parlamento Europeo y del Consejo, los Reglamentos (CE) n.o 1/2005 y (CE) n.o 1099/2009 del Consejo y las Directivas 98/58/CE, 1999/74/CE, 2007/43/CE, 2008/119/CE y 2008/120/CE del Consejo, y por el que se derogan los Reglamentos (CE) n.o 854/2004 y (CE) n.o 882/2004 del Parlamento Europeo y del Consejo, las Directivas 89/608/CEE, 89/662/CEE, 90/425/CEE, 91/496/CEE, 96/23/CE, 96/93/CE y 97/78/CE del Consejo y la Decisión 92/438/CEE del Consejo (Reglamento sobre controles oficiales) (3), y en particular su artículo 90, párrafo primero, letras a) y b), y su artículo 126, apartado 3,
Considerando lo siguiente:
|
(1)
|
El Reglamento de Ejecución (UE) 2020/2235 de la Comisión (4) establece normas relativas a los certificados zoosanitarios previstos en el Reglamento (UE) 2016/429, a los certificados oficiales previstos en el Reglamento (UE) 2017/625 y a los certificados zoosanitarios-oficiales basados en dichos Reglamentos, que se exigen para la entrada en la Unión de determinadas partidas de animales y mercancías (en lo sucesivo denominados conjuntamente «certificados»). En particular, el anexo III del Reglamento de Ejecución (UE) 2020/2235 establece, entre otras cosas, modelos de certificados para la entrada en la Unión de partidas de determinados animales acuáticos vivos y productos de origen animal.
|
|
(2)
|
Más específicamente, los capítulos 1 (MODELO BOV), 2 (MODELO OVI), 24 (MODELO MP-PREP), 25 (MODELO MPNT), 26 (MODELO MPST), 27 (MODELO CAS), 41 (MODELO GEL), 42 (MODELO COL), 43 (MODELO RCG), 44 (MODELO TCG) y 50 (MODELO COMP) del anexo III del Reglamento de Ejecución (UE) 2020/2235 establecen los modelos de certificados zoosanitarios-oficiales, y los certificados oficiales, para la entrada en la Unión de partidas de productos de origen bovino, ovino y caprino. El Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo (5) fue modificado recientemente por el Reglamento (UE) 2021/1176 de la Comisión (6) con el fin de actualizar, entre otras cosas, los requisitos para la entrada en la Unión de productos de origen bovino, ovino y caprino añadiendo condiciones específicas en el caso de la entrada en la Unión de productos derivados de rumiantes procedentes de un país con un riesgo controlado de EEB si provienen de animales originarios de un país con un riesgo indeterminado de EEB. Esos nuevos requisitos para la entrada en la Unión de esas partidas deben reflejarse en dichos modelos de certificados zoosanitarios-oficiales y certificados oficiales. Por tanto, es necesario modificar dichos modelos en consecuencia.
|
|
(3)
|
Además, las certificaciones zoosanitarias y de salud pública que figuran en los modelos de certificados zoosanitarios-oficiales para la entrada en la Unión de partidas de determinadas categorías de productos cárnicos destinados al consumo humano establecidos en los capítulos 25 (MODELO MPNT) y 26 (MODELO MPST) del anexo III del Reglamento de Ejecución (UE) 2020/2235 deben modificarse a fin de que se reflejen con exactitud los requisitos relativos a la entrada en la Unión de productos de origen animal procedentes de cérvidos de cría y silvestres establecidos en el anexo IX, capítulo F, del Reglamento (CE) n.o 999/2001, y el establecimiento de origen de los animales de los que se ha obtenido la carne fresca, establecidos en el artículo 150 del Reglamento Delegado (UE) 2020/692 de la Comisión (7), respectivamente. Por tanto, es necesario modificar dichos modelos en consecuencia.
|
|
(4)
|
En el capítulo 27 del anexo III del Reglamento de Ejecución (UE) 2020/2235 figura un modelo de certificado zoosanitario-oficial para la entrada en la Unión de tripas destinadas al consumo humano (MODELO CAS). De conformidad con el artículo 148 del Reglamento Delegado (UE) 2020/692, el punto II.2.2 de dicho modelo de certificado zoosanitario-oficial prevé la posibilidad, para terceros países o territorios, o zonas de estos, autorizados para la entrada en la Unión de carne fresca y, por tanto, que figuran en el anexo XIII del Reglamento de Ejecución (UE) 2021/404 de la Comisión (8), de introducir en la Unión partidas de tripas sin certificar la aplicación de los tratamientos de reducción del riesgo previstos en el anexo XXVI, punto 2, del Reglamento Delegado (UE) 2020/692. Sin embargo, el texto actual de este punto no es suficientemente claro en lo que se refiere a la zona de origen de las tripas cuando esta posibilidad es aplicable. A fin de aclarar que esta posibilidad solamente se aplica a las zonas enumeradas en el anexo XIII del Reglamento de Ejecución (UE) 2021/404, debe incluirse el código de la zona de origen de las tripas, tal como figura en el anexo XIII del Reglamento de Ejecución (UE) 2021/404. Por consiguiente, es necesario modificar dicho modelo en consecuencia.
|
|
(5)
|
Además, los capítulos 28 (MODELO FISH-CRUST-HC) y 31 (MODELO MOL-HC) del anexo III del Reglamento de Ejecución (UE) 2020/2235 establecen modelos de certificados zoosanitarios-oficiales para la entrada en la Unión de partidas de peces vivos, crustáceos vivos y productos de origen animal procedentes de esos animales destinados al consumo humano, así como partidas de moluscos bivalvos, equinodermos, tunicados, gasterópodos marinos y productos de origen animal vivos derivados de estos animales destinados al consumo humano. A fin de mejorar la claridad de las notas de dichos modelos, debe especificarse claramente que las partidas de productos de origen animal procedentes de animales acuáticos que requieren la cumplimentación de las declaraciones zoosanitarias establecidas en la parte II.2 son aquellas que no han sido excluidas del ámbito de aplicación del Reglamento Delegado (UE) 2020/692, de conformidad con el artículo 1, punto 6, de dicho Reglamento. En concreto, las partidas de productos de origen animal procedentes de animales acuáticos, distintos de los animales acuáticos vivos, que entren en la Unión listos para el consumo humano directo, sin someterse a una transformación ulterior en la Unión, no requieren la cumplimentación de las declaraciones zoosanitarias establecidas en la parte II.2. La definición de «transformación ulterior» también aclarará la situación de dichas partidas. Por tanto, es necesario modificar dichos modelos en consecuencia.
|
|
(6)
|
Además, las recientes modificaciones introducidas en el artículo 167, letras a) y b), y en el artículo 169, apartado 3, letra b), del Reglamento Delegado (UE) 2020/692 mediante el Reglamento Delegado (UE) n.o 2021/1705 de la Comisión (9) deben reflejarse en las declaraciones zoosanitarias de los capítulos 28 (MODELO FISH-CRUST-HC) y 31 (MODELO MOL-HC) del anexo III del Reglamento de Ejecución (UE) 2020/2235. Por tanto, es necesario modificar dichos modelos en consecuencia.
|
|
(7)
|
Además, es necesario aclarar que el período de validez de los modelos de certificados zoosanitarios-oficiales establecidos en los puntos II.2.8 de los capítulos 28 (MODELO FISH-CRUST-HC) y 31 (MODELO MOL-HC) del anexo III del Reglamento de Ejecución (UE) 2020/2235 se aplican únicamente a las partidas de animales acuáticos vivos cubiertas por estos certificados zoosanitarios-oficiales. Por tanto, es necesario modificar dichos modelos en consecuencia.
|
|
(8)
|
Por añadidura, en los capítulos 33, 34 y 35 del anexo III del Reglamento de Ejecución (UE) 2020/2235 se establecen modelos de certificados zoosanitarios-oficiales para la entrada en la Unión de leche cruda destinada al consumo humano (MODELO MILK-RM); productos lácteos destinados al consumo humano derivados de leche cruda o que no han de someterse a un tratamiento específico de reducción del riesgo (MODELO MILK-RMP/NT); y productos lácteos destinados al consumo humano que han de someterse a un tratamiento de pasteurización (MODELO DAIRY-PRODUCTS-PT). Sin embargo, estos modelos no reflejan las alternativas al período de residencia de los animales de los que se obtuvo la leche en el tercer país, territorio o zona de estos de origen de la leche o los productos lácteos, que se establecen en la actualidad en el artículo 154 del Reglamento Delegado (UE) 2020/692, modificado recientemente por el Reglamento Delegado (UE) 2021/1705. Por tanto, es necesario modificar dichos modelos en consecuencia.
|
|
(9)
|
En el capítulo 45 del anexo III del Reglamento de Ejecución (UE) 2020/2235 se establece el modelo de certificado oficial para la entrada en la Unión de partidas de miel y otros productos apícolas destinados al consumo humano (MODELO HON). A fin de garantizar la autenticidad de dichas partidas, deben mejorarse las garantías para estas partidas ajustándolas a determinadas normas establecidas en la Directiva 2001/110/CE del Consejo (10). Por consiguiente, es necesario modificar dicho modelo en consecuencia.
|
|
(10)
|
En los capítulos 50 y 52 del anexo III del Reglamento de Ejecución (UE) 2020/2235 se establece el modelo de certificado zoosanitario-oficial para la entrada en la Unión de productos compuestos perecederos y productos compuestos no perecederos que contengan cualquier cantidad de productos cárnicos, excepto gelatina, colágeno y productos muy refinados, y destinados al consumo humano (MODELO COMP), y el modelo de certificado zoosanitario para el tránsito por la Unión a un tercer país, ya sea mediante tránsito inmediato, o tras almacenamiento en la Unión, de productos compuestos perecederos y productos compuestos no perecederos que contengan cualquier cantidad de productos cárnicos y estén destinados al consumo humano (MODELO TRANSIT-COMP). Ambos modelos incluyen una declaración zoosanitaria específica para los productos lácteos contenidos en los productos compuestos. Por lo que se refiere al lugar de producción, la declaración zoosanitaria no refleja la posibilidad de certificar que los productos lácteos contenidos en los productos compuestos han sido producidos en un Estado miembro. Los productos lácteos producidos en un Estado miembro cumplen todas las garantías zoosanitarias necesarias, por lo que esta posibilidad debe incluirse en dichos modelos. Además, debe modificarse la declaración zoosanitaria para aclarar las diferentes opciones ofrecidas para certificar la especie de origen de la leche a partir de la cual se produjeron los productos lácteos. Por tanto, es necesario modificar dichos modelos en consecuencia.
|
|
(11)
|
Por añadidura, deben modificarse los capítulos 50 (MODELO COMP) y 52 (MODELO TRANSIT-COMP) del anexo III del Reglamento de Ejecución (UE) 2020/2235 para prever la posibilidad de que terceros países o territorios, o zonas de estos, certifiquen diferentes orígenes de los productos transformados contenidos en los productos compuestos, si dichos productos cumplen los requisitos pertinentes en materia de salud pública y sanidad animal. Por tanto, es necesario modificar dichos modelos en consecuencia.
|
|
(12)
|
Procede, por tanto, modificar el anexo III del Reglamento de Ejecución (UE) 2020/2235 en consecuencia.
|
|
(13)
(14)
|
A fin de evitar cualquier perturbación del comercio en lo que respecta a la entrada en la Unión de partidas de determinados animales acuáticos vivos y productos de origen animal, debe seguir autorizándose durante un período transitorio, en determinadas condiciones, el uso de certificados expedidos de conformidad con el Reglamento de Ejecución (UE) 2020/2235, según proceda, antes de las modificaciones introducidas por el presente Reglamento de Ejecución.
Las medidas previstas en el presente Reglamento se ajustan al dictamen del Comité Permanente de Vegetales, Animales, Alimentos y Piensos.
|
HA ADOPTADO EL PRESENTE REGLAMENTO:
Artículo 1
El anexo III del Reglamento de Ejecución (UE) 2020/2235 se modifica de conformidad con el anexo del presente Reglamento.
Artículo 2
Durante un período transitorio hasta el 15 de septiembre de 2022, las partidas de determinados animales acuáticos vivos y productos de origen animal, acompañadas de los certificados zoosanitarios-oficiales, certificados oficiales o certificados zoosanitarios adecuados expedidos de conformidad con los modelos establecidos en los capítulos 1, 2, 24 a 28, 31, 33 a 35, 41 a 45, 50 y 52 del anexo III del Reglamento de Ejecución (UE) 2020/2235, tal como eran aplicables antes de las modificaciones introducidas en dicho Reglamento de Ejecución por el presente Reglamento de Ejecución, seguirán estando autorizadas para su entrada en la Unión a condición de que el certificado haya sido expedido, a más tardar, el 15 de junio de 2022.
Artículo 3
El presente Reglamento entrará en vigor a los veinte días de su publicación en el Diario Oficial de la Unión Europea.
El presente Reglamento será obligatorio en todos sus elementos y directamente aplicable en cada Estado miembro.
Hecho en Bruselas, el 11 de enero de 2022.
Por la Comisión
La Presidenta
Ursula VON DER LEYEN
(1) DO L 139 de 30.4.2004, p. 55.
(2) DO L 84 de 31.3.2016, p. 1.
(3) DO L 95 de 7.4.2017, p. 1.
(4) Reglamento de Ejecución (UE) 2020/2235 de la Comisión, de 16 de diciembre de 2020, por el que se establecen normas para la aplicación de los Reglamentos (UE) 2016/429 y (UE) 2017/625 del Parlamento Europeo y del Consejo por lo que respecta a los modelos de certificados zoosanitarios, los modelos de certificados oficiales y los modelos de certificados zoosanitarios-oficiales para la entrada en la Unión y los desplazamientos dentro de la Unión de las partidas de determinadas categorías de animales y mercancías, así como la certificación oficial relativa a dichos certificados, y se derogan el Reglamento (CE) n.o 599/2004, los Reglamentos de Ejecución (UE) n.o 636/2014 y (UE) 2019/628, la Directiva 98/68/CE y las Decisiones 2000/572/CE, 2003/779/CE y 2007/240/CE (DO L 442 de 30.12.2020, p. 1).
(5) Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo, de 22 de mayo de 2001, por el que se establecen disposiciones para la prevención, el control y la erradicación de determinadas encefalopatías espongiformes transmisibles (DO L 147 de 31.5.2001, p. 1).
(6) Reglamento (UE) 2021/1176 de la Comisión, de 16 de julio de 2021, por el que se modifican los anexos III, V, VII y IX del Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo en lo que respecta al genotipado de casos positivos de EET en las cabras, la determinación de la edad en animales de las especies ovina y caprina, las medidas aplicables en un rebaño o una manada con tembladera atípica y las condiciones para la importación de productos de origen bovino, ovino y caprino (DO L 256 de 19.7.2021, p. 56).
(7) Reglamento Delegado (UE) 2020/692 de la Comisión, de 30 de enero de 2020, que completa el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo en lo referente a las normas para la entrada en la Unión, y para el desplazamiento y la manipulación tras la entrada, de las partidas de determinados animales, productos reproductivos y productos de origen animal (DO L 174 de 3.6.2020, p. 379).
(8) Reglamento de Ejecución (UE) 2021/404 de la Comisión, de 24 de marzo de 2021, por el que se establecen las listas de terceros países, territorios, o zonas de estos, desde los que se permite la entrada en la Unión de animales, productos reproductivos y productos de origen animal de conformidad con el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo (DO L 114 de 31.3.2021, p. 1).
(9) Reglamento Delegado (UE) 2021/1705 de la Comisión, de 14 de julio de 2021, por el que se modifica el Reglamento Delegado (UE) 2020/692, que completa el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo en lo referente a las normas para la entrada en la Unión, y para el desplazamiento y la manipulación tras la entrada, de las partidas de determinados animales, productos reproductivos y productos de origen animal (DO L 339 de 24.9.2021, p. 40).
(10) Directiva 2001/110/CE del Consejo, de 20 de diciembre de 2001, relativa a la miel (DO L 10 de 12.1.2002, p. 47).
ANEXO
El anexo III del Reglamento de Ejecución (UE) 2020/2235 se modifica como sigue:
1) En el capítulo 1, el punto II.1.10 de la declaración sanitaria se sustituye por el texto siguiente:
|
|
|
«II.1.10.
|
en lo referente a la encefalopatía espongiforme bovina (EEB):
|
(1)o bien
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE de la Comisión (A) como país o región con un riesgo insignificante de EEB, y
|
(1)o bien
|
[los animales de los que se han obtenido la carne o la carne picada nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB;]
|
|
(1)o
|
[los animales de los que se han obtenido la carne o la carne picada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y:
|
(1)o bien
|
|
[i)
|
la carne o la carne picada no contienen material especificado de riesgo según se define en el punto 1, letra a), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;]
|
|
|
(1)o
|
|
[i)
|
las canales, las medias canales enteras o cortadas, como máximo, en tres piezas de venta al por mayor y los cuartos de canal no contienen otro material especificado de riesgo, según se define en el punto 1, letra a), del anexo V del Reglamento (CE) n.o 999/2001, que la columna vertebral, incluidos los ganglios de la raíz posterior, y las canales o las piezas de venta al por mayor de canales de animales mayores de treinta meses que contienen la columna vertebral están identificadas por una banda roja claramente visible sobre la etiqueta a la que se refieren los artículos 13 o 15 del Reglamento (CE) n.o 1760/2000 del Parlamento Europeo y del Consejo (B) (3);]
|
|
ii)
|
los animales de los que se han obtenido la carne o la carne picada no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
|
|
(1)o
|
[los animales de los que se han obtenido la carne o la carne picada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
(1)o bien
|
|
[i)
|
la carne o la carne picada no contienen material especificado de riesgo según se define en el punto 1, letra a), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;]
|
|
|
(1)o
|
|
[i)
|
las canales, las medias canales enteras o cortadas, como máximo, en tres piezas de venta al por mayor y los cuartos de canal no contienen otro material especificado de riesgo, según se define en el punto 1, letra a), del anexo V del Reglamento (CE) n.o 999/2001, que la columna vertebral, incluidos los ganglios de la raíz posterior, y las canales o las piezas de venta al por mayor de canales de animales mayores de treinta meses que contienen la columna vertebral están identificadas por una banda roja claramente visible sobre la etiqueta a la que se refieren los artículos 13 o 15 del Reglamento (CE) n.o 1760/2000 (3);]
|
|
ii)
|
los animales de los que se han obtenido la carne o la carne picada no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
iii)
|
los animales de los que se han obtenido la carne o la carne picada no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal (C);
|
|
iv)
|
la carne o la carne picada se han producido y manipulado de una manera que garantiza que no contengan tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se hayan contaminado con ellos;]]
|
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y
|
a)
|
los animales de los que se han obtenido la carne o la carne picada no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal; y
|
|
|
(1)o bien
|
|
[b)
|
la carne o la carne picada no contienen material especificado de riesgo según se define en el punto 1, letra a), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;] y]
|
|
|
(1)o
|
|
[b)
|
las canales, las medias canales enteras o cortadas, como máximo, en tres piezas de venta al por mayor y los cuartos de canal no contienen otro material especificado de riesgo, según se define en el punto 1, letra a), del anexo V del Reglamento (CE) n.o 999/2001, que la columna vertebral, incluidos los ganglios de la raíz posterior, y las canales o las piezas de venta al por mayor de canales de animales mayores de treinta meses que contienen la columna vertebral están identificadas por una banda roja claramente visible sobre la etiqueta a la que se refieren los artículos 13 o 15 del Reglamento (CE) n.o 1760/2000 (3); y]
|
|
|
(1)o bien
|
|
[c)
|
los animales de los que se han obtenido la carne o la carne picada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante o controlado de EEB;]
|
|
|
(1)o
|
|
[c)
|
los animales de los que se han obtenido la carne o la carne picada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
i)
|
los animales de los que se han obtenido la carne o la carne picada no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
ii)
|
la carne o la carne picada se han producido y manipulado de una manera que garantiza que no contengan tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se hayan contaminado con ellos;]]
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
a)
|
los animales de los que se han obtenido la carne o la carne picada no han sido:
|
i)
|
sacrificados, previo aturdimiento, mediante inyección de gas en la cavidad craneal, ni matados con el mismo método, ni sacrificados, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
ii)
|
alimentados con harina de carne y huesos ni chicharrones derivados de rumiantes, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
|
|
(1)o bien
|
|
[b)
|
la carne o la carne picada no contienen material especificado de riesgo según se define en el punto 1, letra a), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;]
|
|
|
(1)o
|
|
[b)
|
las canales, las medias canales enteras o cortadas, como máximo, en tres piezas de venta al por mayor y los cuartos de canal no contienen otro material especificado de riesgo, según se define en el punto 1, letra a), del anexo V del Reglamento (CE) n.o 999/2001, que la columna vertebral, incluidos los ganglios de la raíz posterior, y las canales o las piezas de venta al por mayor de canales de animales mayores de treinta meses que contienen la columna vertebral están identificadas por una banda roja claramente visible sobre la etiqueta a la que se refieren los artículos 13 o 15 del Reglamento (CE) n.o 1760/2000 (3);]
|
|
c)
|
la carne o la carne picada no contienen tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se han obtenido a partir de ellos.]
|
|
|
(A) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84)."
(B) Reglamento (CE) n.o 1760/2000 del Parlamento Europeo y del Consejo, de 17 de julio de 2000, que establece un sistema de identificación y registro de los animales de la especie bovina y relativo al etiquetado de la carne de vacuno y de los productos a base de carne de vacuno y por el que se deroga el Reglamento (CE) n.o 820/97 del Consejo (DO L 204 de 11.8.2000, p. 1)."
(C) https://www.oie.int/es/normas/codigo-terrestre/acceso-en-linea/ »"
|
2) En el capítulo 2, el punto II.1.10 de la declaración sanitaria se sustituye por el texto siguiente:
|
|
|
«II.1.10.
|
en lo referente a la encefalopatía espongiforme bovina (EEB):
|
(1)o bien
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE de la Comisión (D) como país o región con un riesgo insignificante de EEB, y
|
(1)o bien
|
[los animales de los que se han obtenido la carne o la carne picada nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB;]
|
|
(1)o
|
[los animales de los que se han obtenido la carne o la carne picada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y:
i) la carne o la carne picada no contienen material especificado de riesgo según se define en el punto 1, letra b), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;
ii) los animales de los que se han obtenido la carne o la carne picada no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
(1)o
|
[los animales de los que se han obtenido la carne o la carne picada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
i) la carne o la carne picada no contienen material especificado de riesgo según se define en el punto 1, letra b), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;
ii) los animales de los que se han obtenido la carne o la carne picada no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
iii) los animales de los que se han obtenido la carne o la carne picada no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal (E);
iv) la carne o la carne picada se han producido y manipulado de una manera que garantiza que no contengan tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se hayan contaminado con ellos;]
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y
|
a)
|
los animales de los que se han obtenido la carne o la carne picada no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal; y
|
|
b)
|
la carne o la carne picada no contienen material especificado de riesgo según se define en el punto 1, letra b), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material; y
|
|
|
(1)o bien
|
|
[c)
|
los animales de los que se han obtenido la carne o la carne picada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante o controlado de EEB;]
|
|
|
(1)o
|
|
[c)
|
los animales de los que se han obtenido la carne o la carne picada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
i)
|
los animales de los que se han obtenido la carne o la carne picada no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
ii)
|
la carne o la carne picada se han producido y manipulado de una manera que garantiza que no contengan tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se hayan contaminado con ellos;]]
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
a)
|
los animales de los que se han obtenido la carne o la carne picada no han sido:
|
i)
|
sacrificados, previo aturdimiento, mediante inyección de gas en la cavidad craneal, ni matados con el mismo método, ni sacrificados, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
ii)
|
alimentados con harina de carne y huesos ni chicharrones derivados de rumiantes, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
|
b)
|
la carne o la carne picada no contienen ni se han obtenido a partir de:
|
i)
|
material especificado de riesgo como se define en el punto 1, letra b), del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado;]
|
|
|
|
|
(D) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84)."
(E) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/ »"
|
3) El capítulo 24 se modifica como sigue:
|
|
|
a)
|
El punto II.1.11 de la declaración sanitaria se sustituye por el texto siguiente:
|
«(2)
|
|
[II.1.11.
|
si contienen material de bovinos, ovinos o caprinos, en lo referente a la encefalopatía espongiforme bovina (EEB):
|
|
(2)o bien
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE de la Comisión (F) como país o región con un riesgo insignificante de EEB, y
|
(2)o bien
|
[los animales de los que se ha obtenido el preparado de carne nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que no ha habido ningún caso autóctono de EEB;]
|
|
(2)o
|
[los animales de los que se ha obtenido el preparado de carne proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que ha habido al menos un caso autóctono de EEB, y el preparado de carne no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;]
|
|
(2)o
|
[los animales de los que se ha obtenido el preparado de carne proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y:
|
i)
|
el preparado de carne no contiene material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001, ni se ha obtenido a partir de dicho material;
|
|
ii)
|
el preparado de carne no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se ha obtenido el preparado de carne no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
|
(2)o
|
[los animales de los que se ha obtenido el preparado de carne proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
el preparado de carne no contiene material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001, ni se ha obtenido a partir de dicho material;
|
|
ii)
|
el preparado de carne no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se ha obtenido el preparado de carne no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
iv)
|
los animales de los que se ha obtenido el preparado de carne no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal (G);
|
|
v)
|
el preparado de carne se ha producido y manipulado de una manera que garantiza que no contenga tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se haya contaminado con ellos;]]
|
|
|
|
(2)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y
|
a)
|
los animales de los que se ha obtenido el preparado de carne no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
b)
|
el preparado de carne no contiene ni se ha obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos.
|
|
|
|
(2)o bien
|
|
[c)
|
los animales de los que se ha obtenido el preparado de carne proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante o controlado de EEB;]
|
|
|
(2)o
|
|
[c)
|
los animales de los que se ha obtenido el preparado de carne proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
los animales de los que se ha obtenido el preparado de carne no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
ii)
|
el preparado de carne se ha producido y manipulado de una manera que garantiza que no contenga tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se haya contaminado con ellos;]]
|
|
|
|
(2)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
a)
|
los animales de los que se ha obtenido el preparado de carne no han sido:
|
i)
|
sacrificados, previo aturdimiento, mediante inyección de gas en la cavidad craneal, ni matados con el mismo método, ni sacrificados, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
ii)
|
alimentados con harina de carne y huesos ni chicharrones derivados de rumiantes, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
|
b)
|
el preparado de carne no contiene ni se ha obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos;
|
|
iii)
|
tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado.]].
|
|
|
|
(F) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84)."
(G) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/ »"
|
|
b)
|
En las notas, los párrafos introductorios primero y segundo se sustituyen por el texto siguiente:
«De conformidad con el Acuerdo sobre la retirada del Reino Unido de Gran Bretaña e Irlanda del Norte de la Unión Europea y de la Comunidad Europea de la Energía Atómica, y en particular con el artículo 5, apartado 4, del Protocolo sobre Irlanda / Irlanda del Norte, en relación con el anexo 2 de dicho Protocolo, las referencias hechas a la Unión Europea en el presente certificado zoosanitario-oficial incluyen al Reino Unido con respecto a Irlanda del Norte.
El presente certificado zoosanitario-oficial está destinado a la entrada en la Unión de preparados de carne [según se definen en el punto 1.15 del anexo I del Reglamento (CE) n.o 853/2004] elaborados a partir de carne fresca de bovinos, ovinos, caprinos, razas domésticas de porcinos, camélidos, cérvidos, animales de la familia Bovidae distintos de los bovinos, ovinos y caprinos, razas silvestres de porcinos, lepóridos, aves de corral distintas de las ratites, ratites, aves de caza o mamíferos terrestres silvestres distintos de los ungulados y los lepóridos, incluso cuando la Unión no es el destino final del preparado de carne.»
|
|
|
4)
|
El capítulo 25 se modifica como sigue:
|
a)
|
El punto II.1.4.1 de la declaración sanitaria se sustituye por el texto siguiente:
|
«(1) [II.1.4.1.
|
si se han obtenido de carne de porcinos domésticos, dicha carne cumple los requisitos del Reglamento de Ejecución (UE) 2015/1375 de la Comisión (H) y, en particular:
|
(1)o bien
|
[ha sido sometida a examen por un método de digestión para la detección de triquinas, con resultados negativos;]
|
|
(1)o
|
[ha sido sometida a un tratamiento de congelación de conformidad con el anexo II del Reglamento de Ejecución (UE) 2015/1375;]
|
|
(1)(9) o
|
[en el caso de la carne de porcinos domésticos destinados exclusivamente a engorde y sacrificio, procede de una explotación o una categoría de explotaciones reconocidas oficialmente por las autoridades competentes libres de triquinas de conformidad con el anexo IV del Reglamento de Ejecución (UE) 2015/1375;]]
|
|
(H) Reglamento de Ejecución (UE) 2015/1375 de la Comisión, de 10 de agosto de 2015, por el que se establecen normas específicas para los controles oficiales de la presencia de triquinas en la carne (DO L 212 de 11.8.2015, p. 7).»"
|
|
b)
|
El punto II.1.11 de la declaración sanitaria se sustituye por el texto siguiente:
|
«(2) [II.1.11.
|
si contienen material de bovinos, ovinos o caprinos, en lo referente a la encefalopatía espongiforme bovina (EEB):
|
(2)o bien
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE de la Comisión (I) como país o región con un riesgo insignificante de EEB, y
|
|
(2)o bien
|
[los animales de los que se han obtenido los productos cárnicos nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que no ha habido ningún caso autóctono de EEB;]
|
|
(2)o
|
[los animales de los que se han obtenido los productos cárnicos proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que ha habido al menos un caso autóctono de EEB, y los productos cárnicos no contienen carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se han obtenido a partir de dicha carne;]
|
|
(2)o
|
[los animales de los que se han obtenido los productos cárnicos proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y:
|
i)
|
los productos cárnicos no contienen material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;
|
|
ii)
|
los productos cárnicos no contienen carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se han obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se han obtenido los productos cárnicos no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
|
(2)o
|
[los animales de los que se han obtenido los productos cárnicos proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
los productos cárnicos no contienen material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;
|
|
ii)
|
los productos cárnicos no contienen carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se han obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se han obtenido los productos cárnicos no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
iv)
|
los animales de los que se han obtenido los productos cárnicos no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal (J);
|
|
v)
|
los productos cárnicos se han producido y manipulado de una manera que garantiza que no contengan tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se hayan contaminado con ellos;]]
|
|
|
(2)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y
|
a)
|
los animales de los que se han obtenido los productos cárnicos no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
b)
|
los productos cárnicos no contienen ni se han obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos.
|
|
|
|
(2)o bien
|
|
[c)
|
los animales de los que se han obtenido los productos cárnicos proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante o controlado de EEB;]
|
|
|
(2)o
|
|
[c)
|
los animales de los que se han obtenido los productos cárnicos proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
los animales de los que se han obtenido los productos cárnicos no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
ii)
|
los productos cárnicos se han producido y manipulado de una manera que garantiza que no contengan tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se hayan contaminado con ellos;]]
|
|
|
|
(2)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
a)
|
los animales de los que se han obtenido los productos cárnicos no han sido:
|
i)
|
sacrificados, previo aturdimiento, mediante inyección de gas en la cavidad craneal, ni matados con el mismo método, ni sacrificados, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
ii)
|
alimentados con harina de carne y huesos ni chicharrones derivados de rumiantes, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
|
b)
|
los productos cárnicos no contienen ni se han obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos;
|
|
iii)
|
tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado.]]
|
|
|
|
(I) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84)."
(J) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/»"
|
|
c)
|
Después del punto II.1.12, se añaden los puntos II.1.13 y II.1.14 siguientes a la declaración sanitaria:
|
«(1) (10) [II.1.13.
|
si contienen material procedente de cérvidos de cría:
el producto contiene exclusivamente carne, excepto despojos y médula espinal, de cérvidos de cría en los que no se ha detectado caquexia crónica por métodos diagnósticos histopatológicos, inmunohistoquímicos u otros reconocidos por las autoridades competentes, o se ha obtenido exclusivamente a partir de esa carne, y no procede de animales en cuya manada se haya confirmado o se sospeche oficialmente la presencia de esta enfermedad.]
|
|
(1) (11) [II.1.14.
|
si contienen material procedente de cérvidos silvestres:
el producto contiene carne, excepto despojos y médula espinal, de cérvidos silvestres en los que no se ha detectado caquexia crónica por métodos diagnósticos histopatológicos, inmunohistoquímicos u otros reconocidos por las autoridades competentes, o se ha obtenido exclusivamente a partir de esa carne, y no procede de animales provenientes de una región en la que se haya confirmado en los últimos tres años o se sospeche oficialmente la presencia de esta enfermedad.]»
|
|
|
d)
|
Los puntos II.2.5 y II.2.6 de la declaración zoosanitaria se sustituyen por el texto siguiente:
|
«II.2.5.
|
ha sido transformado a partir de carne fresca obtenida de:
|
(1)o bien
|
[animales en cautividad de un establecimiento que no estaba sujeto a medidas de restricción nacionales por motivos zoosanitarios, en particular por las enfermedades pertinentes de la lista mencionadas en el anexo I del Reglamento Delegado (UE) 2020/692 de la Comisión (K) y las enfermedades emergentes en el momento de enviar los animales al matadero, y en el establecimiento y en torno a él, en un radio de 10 km, incluido, cuando proceda, el territorio de un país vecino, no ha habido casos de esas enfermedades en los treinta días previos al envío de los animales a la Unión;]
|
|
(1)o
|
[animales silvestres que procedan de un lugar en el cual y en torno al cual no haya habido casos de ninguna de las enfermedades de la lista pertinentes para la especie de origen de los productos cárnicos de conformidad con el anexo I del Reglamento Delegado (UE) 2020/692 de la Comisión, en los treinta días previos al envío del producto cárnico a la Unión;],
|
|
|
II.2.6.
|
tras su transformación, se ha manipulado hasta su envasado de manera que se evite una contaminación cruzada que pueda introducir un riesgo zoosanitario;
|
|
(8) [II.2.7.
|
está destinado a un Estado miembro al que se ha concedido el estatus de libre de infección por el virus de la enfermedad de Newcastle sin vacunación de conformidad con el Reglamento Delegado (UE) 2020/689 de la Comisión (L), y se ha obtenido de aves de corral que no han sido vacunadas contra la infección por el virus de la enfermedad de Newcastle con una vacuna viva durante los treinta días previos a la fecha de sacrificio.]
|
(K) Reglamento Delegado (UE) 2020/692 de la Comisión, de 30 de enero de 2020, que completa el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo en lo referente a las normas para la entrada en la Unión, y para el desplazamiento y la manipulación tras la entrada, de las partidas de determinados animales, productos reproductivos y productos de origen animal (DO L 174 de 3.6.2020, p. 379)."
(L) Reglamento Delegado (UE) 2020/689 de la Comisión, de 17 de diciembre de 2019, por el que se completa el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo en lo referente a las normas de vigilancia, los programas de erradicación y el estatus de libre de enfermedad con respecto a determinadas enfermedades de la lista y enfermedades emergentes (DO L 174 de 3.6.2020, p. 211). »"
|
|
e)
|
Se añaden las siguientes notas (9) a (11) a las notas de la parte II después de la nota (8):
|
«(9)
|
La excepción relativa a los porcinos domésticos procedentes de una explotación cuyo cumplimiento de las condiciones controladas de estabulación ha sido reconocido oficialmente solo puede ser aplicada en los países enumerados en el anexo VII del Reglamento de Ejecución (UE) 2015/1375.
|
|
(10)
|
Aplicable cuando la carne se ha obtenido de un país mencionado en el punto 1 del capítulo F del anexo IX del Reglamento (CE) n.o 999/2001.
|
|
(11)
|
Aplicable cuando la carne se ha obtenido de un país mencionado en el punto 2 del capítulo F del anexo IX del Reglamento (CE) n.o 999/2001.»
|
|
|
|
5)
|
El capítulo 26 se modifica como sigue:
|
a)
|
El punto II.1.11 de la declaración sanitaria se sustituye por el texto siguiente:
|
«(1)[II.1.11.
|
si contienen material de bovinos, ovinos o caprinos, en lo referente a la encefalopatía espongiforme bovina (EEB):
|
(1)o bien
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE de la Comisión (M) como país o región con un riesgo insignificante de EEB, y
|
|
(1)o bien
|
[los animales de los que se han obtenido los productos cárnicos nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que no ha habido ningún caso autóctono de EEB;]
|
|
(1)o
|
[los animales de los que se han obtenido los productos cárnicos proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que ha habido al menos un caso autóctono de EEB, y los productos cárnicos no contienen carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se han obtenido a partir de dicha carne;]
|
|
(1)o
|
[los animales de los que se han obtenido los productos cárnicos proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y:
|
i)
|
los productos cárnicos no contienen material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;
|
|
ii)
|
los productos cárnicos no contienen carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se han obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se han obtenido los productos cárnicos no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
|
(1)o
|
[los animales de los que se han obtenido los productos cárnicos proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
los productos cárnicos no contienen material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;
|
|
ii)
|
los productos cárnicos no contienen carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se han obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se han obtenido los productos cárnicos no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
iv)
|
los animales de los que se han obtenido los productos cárnicos no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal (N);
|
|
v)
|
los productos cárnicos se han producido y manipulado de una manera que garantiza que no contengan tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se hayan contaminado con ellos;]]
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y
|
a)
|
los animales de los que se han obtenido los productos cárnicos no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
|
(1)o bien
|
|
[b)
|
los productos cárnicos no contienen ni se han obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos;]
|
|
|
|
(1)o
|
|
[b)
|
los productos cárnicos contienen intestinos tratados de animales que nacieron y fueron criados sin interrupción y sacrificados en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que no ha habido ningún caso autóctono de EEB, y se han obtenido a partir de dichos intestinos;]
|
|
|
(1)o
|
|
[b)
|
los productos cárnicos contienen intestinos tratados de animales procedentes de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que ha habido al menos un caso autóctono de EEB, se han obtenido a partir de dichos intestinos y:
|
|
(1)o bien
|
|
[i)
|
los animales nacieron después de la fecha a partir de la cual se ha hecho cumplir la prohibición de alimentar a los rumiantes con harina de carne y huesos y chicharrones obtenidos de rumiantes;]
|
|
|
(1)o bien
|
|
[i)
|
los intestinos tratados de bovino, ovino y caprino no contienen material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.oo 999/2001, ni se han obtenido a partir de dicho material.]]
|
|
|
(1)o bien
|
|
[c)
|
los animales de los que se han obtenido los productos cárnicos proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante o controlado de EEB;]
|
|
|
(1)o
|
|
[c)
|
los animales de los que se han obtenido los productos cárnicos proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
|
i)
|
los animales de los que se han obtenido los productos cárnicos no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
ii)
|
los productos cárnicos se han producido y manipulado de una manera que garantiza que no contengan tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se hayan contaminado con ellos;]]
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
a)
|
los animales de los que se han obtenido los productos cárnicos no han sido:
|
i)
|
sacrificados, previo aturdimiento, mediante inyección de gas en la cavidad craneal, ni matados con el mismo método, ni sacrificados, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
ii)
|
alimentados con harina de carne y huesos ni chicharrones derivados de rumiantes, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
|
|
(1)o bien
|
|
[b)
|
los productos cárnicos no contienen ni se han obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos;
|
|
iii)
|
tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado.]
|
|
|
|
(1)o
|
|
[b)
|
los productos cárnicos contienen intestinos tratados de animales que nacieron y fueron criados sin interrupción y sacrificados en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que no ha habido ningún caso autóctono de EEB, y se han obtenido a partir de dichos intestinos;]
|
|
|
(1)o
|
|
[b)
|
los productos cárnicos contienen intestinos tratados de animales procedentes de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que ha habido al menos un caso autóctono de EEB, se han obtenido a partir de dichos intestinos y:
|
|
|
(1)o bien
|
|
[i)
|
los animales nacieron después de la fecha a partir de la cual se ha hecho cumplir la prohibición de alimentar a los rumiantes con harina de carne y huesos y chicharrones obtenidos de rumiantes;]
|
|
|
(1)o bien
|
|
[i)
|
los intestinos tratados de bovino, ovino y caprino no contienen material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n. oo 999/2001, ni se han obtenido a partir de dicho material.]]]]
|
|
|
(M) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84)."
(N) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/»"
|
|
b)
|
Después del punto II.1.12, se añaden los puntos II.1.13 y II.1.14 siguientes a la declaración sanitaria:
|
«(1) (11)[II.1.13.
|
si contienen material procedente de cérvidos de cría:
el producto contiene exclusivamente carne, excepto despojos y médula espinal, de cérvidos de cría en los que no se ha detectado caquexia crónica por métodos diagnósticos histopatológicos, inmunohistoquímicos u otros reconocidos por las autoridades competentes, o se ha obtenido exclusivamente a partir de esa carne, y no procede de animales en cuya manada se haya confirmado o se sospeche oficialmente la presencia de esta enfermedad.]
|
|
(1) (12)[II.1.14.
|
si contienen material procedente de cérvidos silvestres:
el producto contiene carne, excepto despojos y médula espinal, de cérvidos silvestres en los que no se ha detectado caquexia crónica por métodos diagnósticos histopatológicos, inmunohistoquímicos u otros reconocidos por las autoridades competentes, o se ha obtenido exclusivamente a partir de esa carne, y no procede de animales provenientes de una región en la que se haya confirmado en los últimos tres años o se sospeche oficialmente la presencia de esta enfermedad.]»
|
|
|
c)
|
Los puntos II.2.2 a II.2.4 de la declaración zoosanitaria se sustituyen por el texto siguiente:
|
«(1)o bien
|
|
[II.2.2.
|
ha sido transformado a partir de carne fresca de una única especie animal, con el código ____ (4), y la carne fresca utilizada para la transformación del producto cárnico ha sido sometida al tratamiento específico ____(5), que en la parte 1 del anexo XV del Reglamento de Ejecución (UE) 2021/404 se asigna específicamente a la especie de origen de la carne fresca y a la zona indicada en el punto II.2.1, y se ha obtenido de animales procedentes de:
|
|
(1)o bien
|
[la zona indicada en el punto II.2.1;]]
|
|
(1)o
|
[la zona con el código _____ (6), que, en la fecha de expedición del presente certificado zoosanitario-oficial, figura en la lista para la introducción en la Unión de carne fresca de las especies a partir de las cuales se ha transformado el producto cárnico de
|
(1)o bien
|
[la parte 1 del anexo XIII del Reglamento de Ejecución (UE) 2021/404 de la Comisión, en el caso de la carne fresca de ungulados;]]] (7)
|
|
(1)o
|
[la parte 1 del anexo XIV del Reglamento de Ejecución (UE) 2021/404, en el caso de la carne fresca de aves de corral y aves de caza;]]]
|
|
(1)o
|
[un Estado miembro;]]]
|
|
|
|
(1)o
|
|
[II.2.2.
|
ha sido transformado a partir de carne fresca de aves de corral, con el código ___ (4), procedente de una zona que figura en la lista para la introducción en la Unión de carne fresca de aves de corral y en la que ha habido un caso o un brote de gripe aviar altamente patógena o de infección por el virus de la enfermedad de Newcastle, y la carne fresca utilizada para la transformación del producto cárnico ha sido sometida, como mínimo, al tratamiento específico “D”(5);]
|
|
|
(1)o
|
|
[II.2.2.
|
ha sido transformado mezclando carne fresca de diferentes especies animales, con los códigos ____, ____, ____ (4), y esa carne fresca;
|
|
(1)o bien
|
|
[II.2.2.1.
|
ha sido mezclada antes del tratamiento final y, tras la mezcla, ha sido sometida al tratamiento específico ____(5), pues es el más intenso de los tratamientos que en la parte 1 del anexo XV del Reglamento de Ejecución (UE) 2021/404 se asignan específicamente a las diferentes especies de origen de la carne fresca y a la zona indicada en el punto II.2.1, y se ha obtenido de animales procedentes de:
|
(1)o bien
|
[la zona indicada en el punto II.2.1]]
|
|
(1)o
|
[la zona con
|
(1)
|
[el código _____(6), que, en la fecha de expedición del presente certificado zoosanitario-oficial, figura en la lista de la parte 1 del anexo XIII del Reglamento de Ejecución (UE) 2021/404 para la introducción en la Unión de carne fresca de las especies a partir de las cuales se ha transformado el producto cárnico;](7)
|
|
(1)
|
[el código _____(6), que, en la fecha de expedición del presente certificado zoosanitario-oficial, figura en la lista de la parte 1 del anexo XIV del Reglamento de Ejecución (UE) 2021/404 para la introducción en la Unión de carne fresca de las especies a partir de las cuales se ha transformado el producto cárnico;]]]
|
|
|
(1)o
|
[un Estado miembro;]]
|
|
|
|
(1)o
|
|
[II.2.2.1.
|
ha sido mezclada después del tratamiento final y, antes de la mezcla, ha sido sometida a los tratamientos específicos ________, _________, ________(8), que son los que en la parte 1 del anexo XV del Reglamento de Ejecución (UE) 2021/404 se asignan específicamente a las diferentes especies de origen de la carne fresca y a la zona indicada en el punto II.2.1, y se ha obtenido de animales procedentes de:
|
(1)o bien
|
[la zona indicada en el punto II.2.1;]]
|
|
(1)o
|
[la zona con
|
(1)
|
[el código _____(6), que, en la fecha de expedición del presente certificado zoosanitario-oficial, figura en la lista de la parte 1 del anexo XIII del Reglamento de Ejecución (UE) 2021/404 para la introducción en la Unión de carne fresca de las especies a partir de las cuales se ha transformado el producto cárnico;] (7)
|
|
(1)
|
[el código _____(6), que, en la fecha de expedición del presente certificado zoosanitario-oficial, figura en la lista de la parte 1 del anexo XIV del Reglamento de Ejecución (UE) 2021/404 para la introducción en la Unión de carne fresca de las especies a partir de las cuales se ha transformado el producto cárnico;]]]
|
|
|
(1)o
|
[un Estado miembro;]]
|
|
|
|
|
(1)o
|
|
[II.2.2.
|
ha sido
|
a)
|
transformado a partir de carne fresca de una sola especie animal o mezclando carne fresca de diferentes especies animales, con los códigos ___, ___, ___(4);
|
|
b)
|
transformado a partir de carne fresca obtenida de animales en cautividad de establecimientos situados en las zonas con los códigos ______, _____ , _____(3) que, en la fecha de expedición del presente certificado zoosanitario-oficial, figuran en la lista de la parte 1 del anexo XV del Reglamento de Ejecución (UE) 2021/404 para la introducción en la Unión de productos cárnicos sujetos a la aplicación de uno de los tratamientos específicos definidos en el anexo XXVI del Reglamento Delegado (UE) 2020/692 de la Comisión (O) a la carne fresca de las especies de que se trate;
|
|
c)
|
sometido al tratamiento específico “B”(5);]
|
|
|
II.2.3.
|
ha sido transformado a partir de carne fresca obtenida de:
|
(1)o bien
|
[animales en cautividad de un establecimiento que no estaba sujeto a medidas de restricción nacionales por motivos zoosanitarios, en particular por las enfermedades pertinentes de la lista mencionadas en el anexo I del Reglamento Delegado (UE) 2020/692 de la Comisión y las enfermedades emergentes en el momento de enviar los animales al matadero, y en el establecimiento y en torno a él, en un radio de 10 km, incluido, cuando proceda, el territorio de un país vecino, no ha habido casos de esas enfermedades en los treinta días previos al envío de los animales a la Unión;]
|
|
(1)o
|
[animales silvestres que procedan de un lugar en el cual y en torno al cual no haya habido casos de ninguna de las enfermedades de la lista pertinentes para la especie de origen de los productos cárnicos de conformidad con el anexo I del Reglamento Delegado (UE) 2020/692 de la Comisión, en los treinta días previos al envío del producto cárnico a la Unión;],
|
|
|
II.2.4.
|
tras su transformación, se ha manipulado hasta su envasado de manera que se evite una contaminación cruzada que pueda introducir un riesgo zoosanitario;
|
|
(9)[II.2.5.
|
está destinado a un Estado miembro al que se ha concedido el estatus de libre de infección por el virus de la enfermedad de Newcastle sin vacunación de conformidad con el Reglamento Delegado (UE) 2020/689 de la Comisión (P), y se ha obtenido de aves de corral que no han sido vacunadas contra la infección por el virus de la enfermedad de Newcastle con una vacuna viva durante los treinta días previos a la fecha de sacrificio].
|
|
(O) Reglamento Delegado (UE) 2020/692 de la Comisión, de 30 de enero de 2020, que completa el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo en lo referente a las normas para la entrada en la Unión, y para el desplazamiento y la manipulación tras la entrada, de las partidas de determinados animales, productos reproductivos y productos de origen animal (DO L 174 de 3.6.2020, p. 379)."
(P) Reglamento Delegado (UE) 2020/689 de la Comisión, de 17 de diciembre de 2019, por el que se completa el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo en lo referente a las normas de vigilancia, los programas de erradicación y el estatus de libre de enfermedad con respecto a determinadas enfermedades de la lista y enfermedades emergentes (DO L 174 de 3.6.2020, p. 211). »"
|
|
d)
|
Después de la nota (10) se añaden las siguientes notas (11) y (12) a las notas de la parte II:
|
«(11)
|
Aplicable cuando la carne se ha obtenido de un país mencionado en el punto 1 del capítulo F del anexo IX del Reglamento (CE) n.o 999/2001.
|
|
(12)
|
Aplicable cuando la carne se ha obtenido de un país mencionado en el punto 2 del capítulo F del anexo IX del Reglamento (CE) n.o 999/2001.»
|
|
|
|
6)
|
El capítulo 27 se modifica como sigue:
|
a)
|
El punto II.1.7 de la declaración sanitaria se sustituye por el texto siguiente:
|
«(1)[II.1.7.
|
si proceden de bovinos, ovinos o caprinos, en lo referente a la encefalopatía espongiforme bovina (EEB):
|
(1)o bien
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE de la Comisión (Q) como país o región con un riesgo insignificante de EEB, y(4)
|
(1)
|
[los animales de los que se han obtenido las tripas nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB;]
|
|
(1)
|
[los animales de los que se han obtenido las tripas proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y:
|
i)
|
si se han obtenido de bovinos, las tripas no contienen material especificado de riesgo según se define en el punto 1, letra a), inciso iii), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;
|
|
ii)
|
los animales de los que se han obtenido las tripas no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
|
(1)
|
[los animales de los que se han obtenido las tripas proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
si se han obtenido de bovinos, las tripas no contienen material especificado de riesgo según se define en el punto 1, letra a), inciso iii), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;
|
|
ii)
|
los animales de los que se han obtenido las tripas no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
iii)
|
los animales de los que se han obtenido las tripas no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal (R);]]
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y (4)
|
(1)
|
[los animales de los que se han obtenido las tripas nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que no ha habido ningún caso autóctono de EEB;]
|
|
(1)
|
[los animales de los que se han obtenido las tripas nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que ha habido al menos un caso autóctono de EEB y, si las tripas se han obtenido de bovinos:
|
i)
|
los animales nacieron después de la fecha a partir de la cual se ha hecho cumplir la prohibición de alimentar a los rumiantes con harina de carne y huesos y chicharrones obtenidos de rumiantes,
|
|
ii)
|
o las tripas no contienen material especificado de riesgo según se define en el punto 1, letra a), inciso iii), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material.]
|
|
|
(1)
|
[los animales de los que se han obtenido las tripas proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y:
|
i)
|
los animales de los que se han obtenido las tripas no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal,
|
|
ii)
|
si se han obtenido de bovinos, las tripas no contienen material especificado de riesgo según se define en el punto 1, letra a), inciso iii), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;]
|
|
|
(1)
|
[los animales de los que se han obtenido las tripas proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
i)
|
los animales de los que se han obtenido las tripas no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal,
|
|
ii)
|
los animales de los que se han obtenido las tripas no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal,
|
|
iii)
|
si se han obtenido de bovinos, las tripas no contienen material especificado de riesgo según se define en el punto 1, letra a), inciso iii), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;]]
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y(4)
|
(1)
|
[las tripas y los animales de los que se han obtenido las tripas cumplen los requisitos siguientes:
|
i)
|
los animales de los que se han obtenido las tripas no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
ii)
|
los animales de los que se han obtenido las tripas no han sido alimentados con harina de carne y huesos ni chicharrones derivados de rumiantes, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal,
|
|
iii)
|
si se han obtenido de bovinos, las tripas no contienen material especificado de riesgo según se define en el punto 1, letra a), inciso iii), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material;]
|
|
|
(1)
|
[los animales de los que se han obtenido las tripas nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que no ha habido ningún caso autóctono de EEB;]
|
|
(1)
|
[los animales de los que se han obtenido las tripas proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que ha habido al menos un caso autóctono de EEB y, si las tripas se han obtenido de bovinos:
|
i)
|
los animales nacieron después de la fecha a partir de la cual se ha hecho cumplir la prohibición de alimentar a los rumiantes con harina de carne y huesos y chicharrones obtenidos de rumiantes,
|
|
ii)
|
o las tripas no contienen material especificado de riesgo según se define en el punto 1, letra a), inciso iii), del anexo V del Reglamento (CE) n.o 999/2001, ni se han obtenido a partir de dicho material.]]]
|
|
|
|
(Q) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84)."
(R) https://www.oie.int/es/normas/codigo-terrestre/acceso-en-linea/»"
|
|
b)
|
El punto II.2.2 de la declaración zoosanitaria se sustituye por el texto siguiente:
|
«(1)o bien
|
|
[II.2.2.
|
han sido:
|
a)
|
transformadas a partir de vejigas o intestinos obtenidos de [bovinos](1), [ovinos o caprinos](1), [porcinos en cautividad](1), y
|
|
b)
|
transformadas en las zonas con los siguientes códigos, y expedidas desde ellas: _______ (3), que, en la fecha de expedición del presente certificado zoosanitario-oficial, están autorizadas para la introducción en la Unión de carne fresca de esas especies animales y figuran en la lista de la parte 1 del anexo XIII del Reglamento de Ejecución (UE) 2021/404, sin ninguna condición específica indicada en la columna 5 del cuadro de la parte 1 de dicho anexo;]
|
|
|
|
(1)o
|
|
[II.2.2.
|
han sido transformadas a partir de vejigas o intestinos obtenidos de [bovinos](1), [ovinos o caprinos](1), [porcinos en cautividad](1), y durante su transformación han sido sometidas:
|
(1)o bien
|
[a saladura con cloruro de sodio (NaCl), o bien seco, o bien como salmuera saturada (aw < 0,80), durante un período ininterrumpido de treinta días o más, a una temperatura igual o superior a 20 °C;]]
|
|
(1)o
|
[a saladura con sal fosfatada con un 86,5 % de NaCl, un 10,7 % de Na2HPO4 y un 2,8 % de Na3PO4 (peso/peso/peso), o bien seca, o bien como salmuera saturada (aw < 0,80), durante un período ininterrumpido de treinta días o más, a una temperatura igual o superior a 20 °C;]]
|
|
|
|
(1)o
|
|
[II.2.2.
|
han sido transformadas a partir de vejigas o intestinos obtenidos de animales distintos de bovinos, ovinos, caprinos o porcinos, y durante su transformación han sido sometidas:
|
(1)o bien
|
[a saladura con cloruro de sodio (NaCl) durante treinta días;]]
|
|
(1)o
|
[a secado tras el raspado;]]»
|
|
|
|
|
|
7)
|
El capítulo 28 se modifica como sigue:
|
a)
|
La declaración zoosanitaria se modifica como sigue:
|
i)
|
El punto II.2.3.3 se sustituye por el texto siguiente:
|
«II.2.3.3.
|
Son animales acuáticos que se expiden directamente a la Unión desde su lugar de origen.»
|
|
|
ii)
|
El punto II.2.6.3 se sustituye por el texto siguiente:
|
«II.2.6.3.
|
desde el momento de la carga en el lugar de origen hasta el momento de llegada a la Unión, los animales de la partida no son transportados en la misma agua ni el mismo (4)[recipiente] (4)[buque vivero] que animales acuáticos de situación sanitaria inferior o no destinados a entrar en la Unión;»
|
|
|
iii)
|
Los puntos II.2.7.3 y II.2.8 se sustituyen por el texto siguiente:
|
«(4)[II.2.7.3.
|
En el caso de los productos de origen animal procedentes de animales acuáticos que no sean animales acuáticos vivos, la etiqueta legible y visible a la que se refiere el punto II.2.7.1 contiene uno de los siguientes enunciados:
|
a)
|
“peces destinados al consumo humano, tras una transformación ulterior en la Unión Europea”;
|
|
b)
|
“crustáceos destinados al consumo humano, tras una transformación ulterior en la Unión Europea”.]
|
|
|
(4) (10)II.2.8.
|
Validez del certificado zoosanitario-oficial
|
El presente certificado zoosanitario-oficial será válido durante diez días a partir de la fecha de expedición. En caso de transporte de animales acuáticos por vía navegable o mar, este período de diez días podrá ampliarse tanto como dure el viaje por vía navegable o mar.»
|
|
|
b)
|
Las notas se modifican como sigue:
|
i)
|
En la parte introductoria, se añade la descripción siguiente de “Transformación ulterior” después de la descripción de “Animales de acuicultura”:
«La “transformación ulterior” es cualquier tipo de medidas y técnicas realizadas antes de la comercialización para el consumo humano que afecten a la integridad anatómica, como el sangrado, la evisceración, el descabezado, el corte en rodajas y el fileteado, que produzcan residuos o subproductos que puedan provocar un riesgo de propagación de enfermedades.»
|
|
ii)
|
La nota 2 de las notas de la parte II se sustituye por el texto siguiente:
|
«(2)
|
La parte II.2 del presente certificado zoosanitario-oficial no será aplicable, y deberá suprimirse, cuando la partida se componga de: a) especies distintas de las enumeradas en el anexo del Reglamento de Ejecución (UE) 2018/1882 de la Comisión (S); o b) animales acuáticos silvestres y productos de origen animal procedentes de esos animales acuáticos, que se desembarquen de buques pesqueros para el consumo humano directo; o c) productos de origen animal procedentes de animales acuáticos que no sean animales acuáticos vivos, que estén listos para el consumo humano directo sin ser sometidos a una transformación ulterior en la Unión.
|
(S) Reglamento de Ejecución (UE) 2018/1882 de la Comisión, de 3 de diciembre de 2018, relativo a la aplicación de determinadas normas de prevención y control a categorías de enfermedades enumeradas en la lista y por el que se establece una lista de especies y grupos de especies que suponen un riesgo considerable para la propagación de dichas enfermedades de la lista (DO L 308 de 4.12.2018, p. 21). »"
|
|
iii)
|
La nota 10 de las notas de la parte II se sustituye por el texto siguiente:
|
«(10)
|
Solo se aplicará a las partidas de animales acuáticos vivos.
|
|
(11)
|
Debe ir firmado por:
|
—
|
un veterinario oficial, cuando no se suprima la parte II.2 “Declaración zoosanitaria”,
|
|
—
|
un agente certificador o un veterinario oficial, cuando se suprima la parte II.2 “Declaración zoosanitaria”.»
|
|
|
|
|
|
8)
|
El capítulo 31 se modifica como sigue:
|
a)
|
La declaración zoosanitaria se modifica como sigue:
|
i)
|
El punto II.2.3.3 se sustituye por el texto siguiente:
|
«II.2.3.3.
|
Son animales acuáticos que se expiden directamente a la Unión desde su lugar de origen.»
|
|
|
ii)
|
El punto II.2.6.3 se sustituye por el texto siguiente:
|
«II.2.6.3.
|
desde el momento de la carga en el lugar de origen hasta el momento de llegada a la Unión, los animales de la partida no son transportados en la misma agua ni el mismo (4)[recipiente] (4)[buque vivero] que animales acuáticos de situación sanitaria inferior o no destinados a entrar en la Unión;»
|
|
|
iii)
|
El punto II.2.8 se sustituye por el texto siguiente:
|
(4) (10)
|
|
«II.2.8.
|
Validez del certificado zoosanitario-oficial
|
El presente certificado zoosanitario-oficial será válido durante diez días a partir de la fecha de expedición. En caso de transporte de animales acuáticos por vía navegable o mar, este período de diez días podrá ampliarse tanto como dure el viaje por vía navegable o mar.»
|
|
|
|
b)
|
Las notas se modifican como sigue:
|
i)
|
En la parte introductoria, se añade la descripción siguiente de “Transformación ulterior” después de la descripción de “Animales de acuicultura”:
«La “transformación ulterior” es cualquier tipo de medidas y técnicas realizadas antes de la comercialización para el consumo humano que afecten a la integridad anatómica, como el sangrado, la evisceración, el descabezado, el corte en rodajas y el fileteado, que produzcan residuos o subproductos que puedan provocar un riesgo de propagación de enfermedades.»
|
|
ii)
|
La nota 2 de las notas de la parte II se sustituye por el texto siguiente:
|
«(2)
|
La parte II.2 del presente certificado zoosanitario-oficial no será aplicable, y deberá suprimirse, cuando la partida se componga de: a) especies distintas de las enumeradas en el anexo del Reglamento de Ejecución (UE) 2018/1882 de la Comisión (T); o b) animales acuáticos silvestres y productos de origen animal procedentes de esos animales acuáticos, que se desembarquen de buques pesqueros para el consumo humano directo; o c) productos de origen animal procedentes de animales acuáticos que no sean animales acuáticos vivos, que estén listos para el consumo humano directo sin ser sometidos a una transformación ulterior en la Unión.
|
(T) Reglamento de Ejecución (UE) 2018/1882 de la Comisión, de 3 de diciembre de 2018, relativo a la aplicación de determinadas normas de prevención y control a categorías de enfermedades enumeradas en la lista y por el que se establece una lista de especies y grupos de especies que suponen un riesgo considerable para la propagación de dichas enfermedades de la lista (DO L 308 de 4.12.2018, p. 21).»"
|
|
iii)
|
La nota 10 de las notas de la parte II se sustituye por el texto siguiente:
|
«(10)
|
Solo se aplicará a las partidas de animales acuáticos vivos.
|
|
(11)
|
Debe ir firmado por:
|
—
|
un veterinario oficial, cuando no se suprima la parte II.2 “Declaración zoosanitaria”,
|
|
—
|
un agente certificador o un veterinario oficial, cuando se suprima la parte II.2 “Declaración zoosanitaria”.»
|
|
|
|
|
|
9)
|
En el capítulo 33, el punto II.2.2 de la declaración zoosanitaria se sustituye por el texto siguiente:
|
«II.2.2.
|
se ha obtenido de animales de la especie [Bos Taurus,](1) [Ovis aries,](1) [Capra hircus,](1) [Bubalus bubalis,](1) [Camelus dromedarius](1) que:
|
(1)o bien
|
[han permanecido en la zona o las zonas indicadas en el punto II.2.1 desde su nacimiento o, como mínimo, durante los tres meses previos a la fecha de ordeño;]
|
|
(1)o
|
[han sido introducidos en la zona o las zonas indicadas en el punto II.2.1 desde:
|
(1)o bien
|
[otro tercer país, territorio o zona de estos que figure en la lista para la entrada en la Unión de leche cruda, calostro o productos a base de calostro, y los animales hayan permanecido en ellos por lo menos durante los tres meses previos a la fecha de ordeño;]]
|
|
(1)o
|
[un Estado miembro;]]»
|
|
|
|
|
10)
|
En el capítulo 34, el punto II.2.3 de la declaración zoosanitaria se sustituye por el texto siguiente:
|
«II.2.3.
|
han sido transformados a partir de leche cruda obtenida de animales de la especie [Bos Taurus,](1) [Ovis aries,](1) [Capra hircus,](1) [Bubalus bubalis,](1) [Camelus dromedarius](1) que:
|
(1)o bien
|
[han permanecido en la zona o las zonas indicadas en el punto II.2.1 desde su nacimiento o, como mínimo, durante los tres meses previos a la fecha de ordeño;]
|
|
(1)o
|
[han sido introducidos en la zona o las zonas indicadas en el punto II.2.1 desde:
|
(1)o bien
|
[otro tercer país, territorio o zona de estos que figure en la lista para la entrada en la Unión de leche cruda, calostro o productos a base de calostro, y los animales hayan permanecido en ellos por lo menos durante los tres meses previos a la fecha de ordeño;]]
|
|
(1)o
|
[un Estado miembro;]]»
|
|
|
|
|
11)
|
En el capítulo 35, el punto II.2.3 de la declaración zoosanitaria se sustituye por el texto siguiente:
|
«II.2.3.
|
han sido transformados a partir de leche cruda obtenida de animales de la especie [Bos Taurus,](1) [Ovis aries,](1) [Capra hircus,](1) [Bubalus bubalis,](1) [Camelus dromedarius](1) que:
|
(1)o bien
|
[han permanecido en la zona o las zonas indicadas en el punto II.2.1 desde su nacimiento o, como mínimo, durante los tres meses previos a la fecha de ordeño;]
|
|
(1)o
|
[han sido introducidos en la zona o las zonas indicadas en el punto II.2.1 desde:
|
(1)o bien
|
[otro tercer país, territorio o zona de estos que figure en la lista para la entrada en la Unión de leche cruda, calostro o productos a base de calostro, y los animales hayan permanecido en ellos por lo menos durante los tres meses previos a la fecha de ordeño;]]
|
|
(1)o
|
[un Estado miembro;]]»
|
|
|
|
|
12)
|
En el capítulo 41, el punto II.1.6 de la declaración sanitaria se sustituye por el texto siguiente:
|
«(1)[II.1.6.
|
en el caso de la gelatina de bovino, ovino y caprino, y con excepción de la gelatina derivada de cueros y pieles:
|
|
(1)o bien
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE de la Comisión (U) como país o región con un riesgo insignificante de encefalopatía espongiforme bovina (EEB), y(2)
|
(1)
|
[los animales de los que se ha obtenido la gelatina nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que no ha habido ningún caso autóctono de EEB;]
|
|
(1)
|
[los animales de los que se ha obtenido la gelatina proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que ha habido al menos un caso autóctono de EEB, y la gelatina no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;]
|
|
(1)
|
[los animales de los que se ha obtenido la gelatina proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y:
|
i)
|
la gelatina no contiene material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo (V), ni se ha obtenido a partir de dicho material;
|
|
ii)
|
la gelatina no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se ha obtenido la gelatina no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
|
(1)
|
[los animales de los que se ha obtenido la gelatina proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
la gelatina no contiene material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001, ni se ha obtenido a partir de dicho material;
|
|
ii)
|
la gelatina no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se ha obtenido la gelatina no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
iv)
|
los animales de los que se ha obtenido la gelatina no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal (W);
|
|
v)
|
la gelatina se ha producido y manipulado de una manera que garantiza que no contenga tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se haya contaminado con ellos;]]
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y
|
a)
|
los animales de los que se ha obtenido la gelatina no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
b)
|
la gelatina no contiene ni se ha obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos.
|
|
|
|
(1)o bien
|
|
[c)
|
los animales de los que se ha obtenido la gelatina proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante o controlado de EEB;]
|
|
|
(1)o
|
|
[c)
|
los animales de los que se ha obtenido la gelatina proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
i)
|
los animales de los que se ha obtenido la gelatina no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
ii)
|
la gelatina se ha producido y manipulado de una manera que garantiza que no contenga tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se haya contaminado con ellos;]]
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
a)
|
los animales de los que se ha obtenido la gelatina no han sido:
|
i)
|
sacrificados, previo aturdimiento, mediante inyección de gas en la cavidad craneal, ni matados con el mismo método, ni sacrificados, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
ii)
|
alimentados con harina de carne y huesos ni chicharrones derivados de rumiantes, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
|
b)
|
la gelatina no contiene ni se ha obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos;
|
|
iii)
|
tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado.]]
|
|
|
(U) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84)."
(V) Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo, de 22 de mayo de 2001, por el que se establecen disposiciones para la prevención, el control y la erradicación de determinadas encefalopatías espongiformes transmisibles (DO L 147 de 31.5.2001, p. 1)."
(W) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/»"
|
|
13)
|
En el capítulo 42, el punto II.1.6 de la declaración sanitaria se sustituye por el texto siguiente:
|
«(1)[II.1.6.
|
en el caso del colágeno de bovino, ovino y caprino, y con excepción del colágeno derivado de cueros y pieles:
|
|
(1)o bien
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE de la Comisión (X) como país o región con un riesgo insignificante de encefalopatía espongiforme bovina (EEB), y(2)
|
(1)
|
[los animales de los que se ha obtenido el colágeno nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que no ha habido ningún caso autóctono de EEB;]
|
|
(1)
|
[los animales de los que se ha obtenido el colágeno proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que ha habido al menos un caso autóctono de EEB, y el colágeno no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;]
|
|
(1)
|
[los animales de los que se ha obtenido el colágeno proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y:
|
i)
|
el colágeno no contiene material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo (Y), ni se ha obtenido a partir de dicho material;
|
|
ii)
|
el colágeno no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se ha obtenido el colágeno no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
|
(1)
|
[los animales de los que se ha obtenido el colágeno proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
el colágeno no contiene material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001, ni se ha obtenido a partir de dicho material;
|
|
ii)
|
el colágeno no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se ha obtenido el colágeno no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
iv)
|
los animales de los que se ha obtenido el colágeno no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal (Z);
|
|
v)
|
el colágeno se ha producido y manipulado de una manera que garantiza que no contenga tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se haya contaminado con ellos;]]
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y
|
a)
|
los animales de los que se ha obtenido el colágeno no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
b)
|
el colágeno no contiene ni se ha obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos.
|
|
|
(1)o bien
|
|
[c)
|
los animales de los que se ha obtenido el colágeno proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante o controlado de EEB;]
|
|
|
(1)o
|
|
[c)
|
los animales de los que se ha obtenido el colágeno proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
i)
|
los animales de los que se ha obtenido el colágeno no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
ii)
|
el colágeno se ha producido y manipulado de una manera que garantiza que no contenga tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se haya contaminado con ellos;]]
|
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
a)
|
los animales de los que se ha obtenido el colágeno no han sido:
|
i)
|
sacrificados, previo aturdimiento, mediante inyección de gas en la cavidad craneal, ni matados con el mismo método, ni sacrificados, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
ii)
|
alimentados con harina de carne y huesos ni chicharrones derivados de rumiantes, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
|
b)
|
el colágeno no contiene ni se ha obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos;
|
|
iii)
|
tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado.]]
|
|
|
(X) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84)."
(Y) Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo, de 22 de mayo de 2001, por el que se establecen disposiciones para la prevención, el control y la erradicación de determinadas encefalopatías espongiformes transmisibles (DO L 147 de 31.5.2001, p. 1)."
(Z) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/»"
|
|
14)
|
En el capítulo 43, el punto II.1.4 de la declaración sanitaria se sustituye por el texto siguiente:
|
«(1)[II.1.4.
|
en el caso de materias primas de bovino, ovino y caprino, y con excepción de los cueros y las pieles:
|
(1)o bien
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE de la Comisión (AA) como país o región con un riesgo insignificante de encefalopatía espongiforme bovina (EEB), y(7)
|
(1)
|
[los animales de los que se ha obtenido la materia prima nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que no ha habido ningún caso autóctono de EEB;]
|
|
(1)
|
[los animales de los que se ha obtenido la materia prima proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que ha habido al menos un caso autóctono de EEB, y la materia prima no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;]
|
|
(1)
|
[los animales de los que se ha obtenido la materia prima proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y:
|
i)
|
la materia prima no contiene material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001, ni se ha obtenido a partir de dicho material;
|
|
ii)
|
la materia prima no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se ha obtenido la materia prima no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
|
(1)
|
[los animales de los que se ha obtenido la materia prima proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
la materia prima no contiene material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001, ni se ha obtenido a partir de dicho material;
|
|
ii)
|
la materia prima no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se ha obtenido la materia prima no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
iv)
|
los animales de los que se ha obtenido la materia prima no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal (BB);
|
|
v)
|
la materia prima se ha producido y manipulado de una manera que garantiza que no contenga tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se haya contaminado con ellos;]]
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y
|
a)
|
los animales de los que se ha obtenido la materia prima no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
b)
|
la materia prima no contiene ni se ha obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos.
|
|
|
|
(1)o bien
|
|
[c)
|
los animales de los que se ha obtenido la materia prima proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante o controlado de EEB;]
|
|
|
(1)o
|
|
[c)
|
los animales de los que se ha obtenido la materia prima proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
los animales de los que se ha obtenido la materia prima no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
ii)
|
la materia prima se ha producido y manipulado de una manera que garantiza que no contenga tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se haya contaminado con ellos;]]
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
a)
|
los animales de los que se ha obtenido la materia prima no han sido:
|
i)
|
sacrificados, previo aturdimiento, mediante inyección de gas en la cavidad craneal, ni matados con el mismo método, ni sacrificados, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
ii)
|
alimentados con harina de carne y huesos ni chicharrones derivados de rumiantes, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
|
b)
|
la materia prima no contiene ni se ha obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos;
|
|
iii)
|
tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado.]]
|
|
|
|
|
(AA) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84)."
(BB) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/»"
|
15) En el capítulo 44, el punto II.1.7 de la declaración sanitaria se sustituye por el texto siguiente:
|
|
|
«(1)–[II.1.7.
|
en el caso de materias primas tratadas de bovino, ovino y caprino, y con excepción de los cueros y las pieles:
|
|
(1)o bien
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE de la Comisión (CC) como país o región con un riesgo insignificante de encefalopatía espongiforme bovina (EEB), y(5)
|
(1)
|
[los animales de los que se ha obtenido la materia prima tratada nacieron, se criaron ininterrumpidamente y se sacrificaron en un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que no ha habido ningún caso autóctono de EEB;]
|
|
(1)
|
[los animales de los que se ha obtenido la materia prima tratada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante de EEB y en los que ha habido al menos un caso autóctono de EEB, y la materia prima tratada no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;]
|
|
(1)
|
[los animales de los que se ha obtenido la materia prima tratada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y:
|
i)
|
la materia prima tratada no contiene material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo (DD), ni se ha obtenido a partir de dicho material;
|
|
ii)
|
la materia prima tratada no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se ha obtenido la materia prima tratada no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
|
(1)
|
[los animales de los que se ha obtenido la materia prima tratada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
la materia prima tratada no contiene material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001, ni se ha obtenido a partir de dicho material;
|
|
ii)
|
la materia prima tratada no contiene carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos, ni se ha obtenido a partir de dicha carne;
|
|
iii)
|
los animales de los que se ha obtenido la materia prima tratada no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;]
|
|
iv)
|
los animales de los que se ha obtenido la materia prima tratada no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal (EE);
|
|
v)
|
la materia prima tratada se ha producido y manipulado de una manera que garantiza que no contenga tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se haya contaminado con ellos;]]
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo controlado de EEB, y
|
a)
|
los animales de los que se ha obtenido la materia prima tratada no se sacrificaron, previo aturdimiento, por inyección de gas en la cavidad craneal, ni se mataron con el mismo método, ni se sacrificaron, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
b)
|
la materia prima tratada no contiene ni se ha obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos.
|
|
|
|
(1)o bien
|
|
[c)
|
los animales de los que se ha obtenido la materia prima tratada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo insignificante o controlado de EEB;]
|
|
|
(1)o
|
|
[c)
|
los animales de los que se ha obtenido la materia prima tratada proceden de un país o una región clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y:
|
i)
|
los animales de los que se ha obtenido la materia prima tratada no han sido alimentados con harina de carne y huesos ni chicharrones, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
ii)
|
la materia prima tratada se ha producido y manipulado de una manera que garantiza que no contenga tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado ni se haya contaminado con ellos;]]
|
|
|
|
(1)o
|
[el país o la región de origen están clasificados de conformidad con la Decisión 2007/453/CE como país o región con un riesgo indeterminado de EEB, y
|
a)
|
los animales de los que se ha obtenido la materia prima tratada no han sido:
|
i)
|
sacrificados, previo aturdimiento, mediante inyección de gas en la cavidad craneal, ni matados con el mismo método, ni sacrificados, previo aturdimiento, por laceración del tejido nervioso central mediante la introducción de un instrumento en forma de vara alargada en la cavidad craneal;
|
|
ii)
|
alimentados con harina de carne y huesos ni chicharrones derivados de rumiantes, según se definen en el Código Sanitario para los Animales Terrestres de la Organización Mundial de Sanidad Animal;
|
|
|
b)
|
la materia prima tratada no contiene ni se ha obtenido a partir de:
|
i)
|
material especificado de riesgo según se define en el punto 1 del anexo V del Reglamento (CE) n.o 999/2001;
|
|
ii)
|
carne separada mecánicamente obtenida de huesos de bovinos, ovinos y caprinos;
|
|
iii)
|
tejidos nerviosos y linfáticos expuestos durante el proceso de deshuesado.]]
|
|
|
|
(CC) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84)."
(DD) Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo, de 22 de mayo de 2001, por el que se establecen disposiciones para la prevención, el control y la erradicación de determinadas encefalopatías espongiformes transmisibles (DO L 147 de 31.5.2001, p. 1)."
(EE) https://www.oie.int/en/standard-setting/terrestrial-code/access-online»"
|
16) El capítulo 45 se sustituye por el texto siguiente:
«
|
17)
|
El capítulo 50 se sustituye por el texto siguiente: « 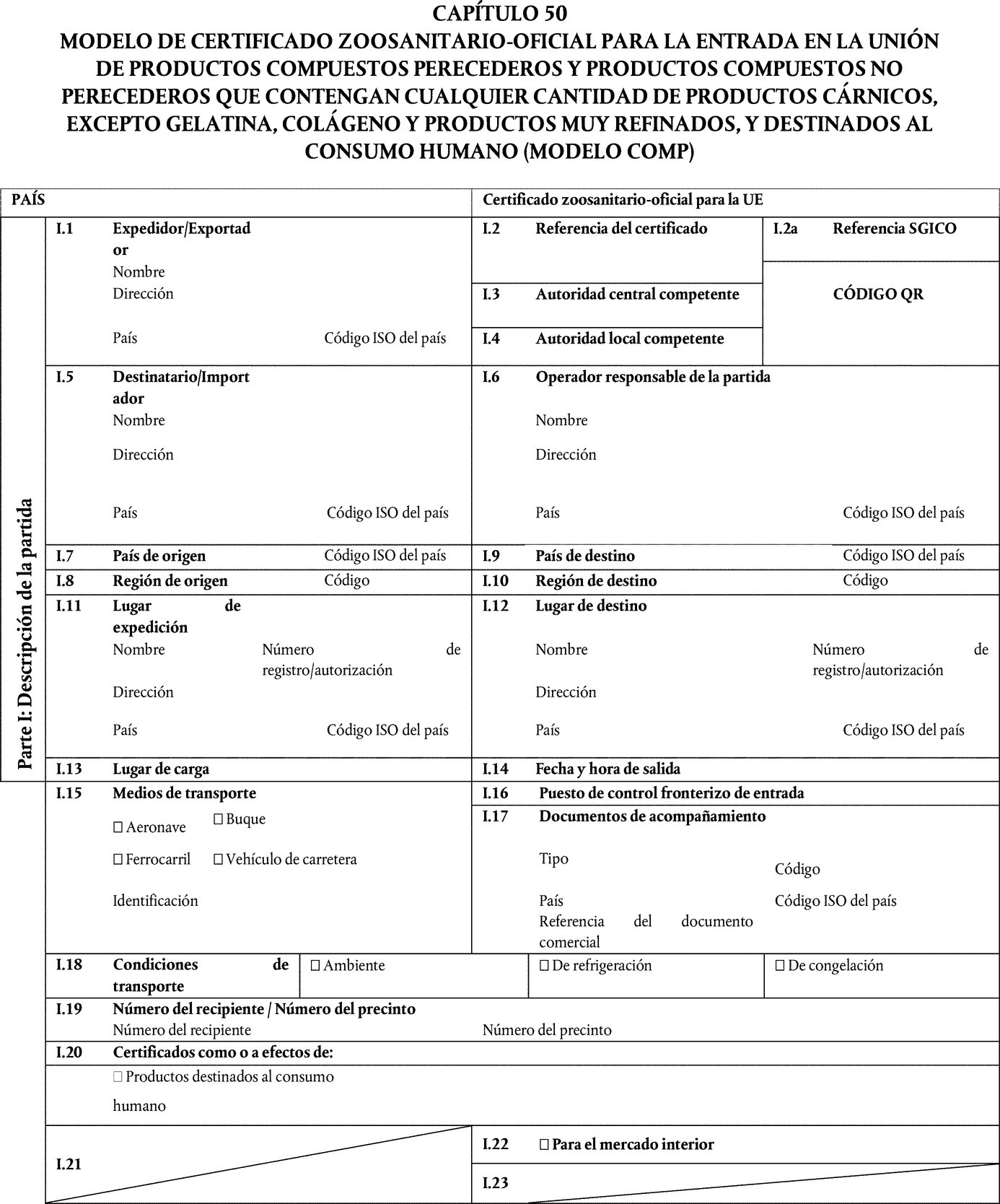 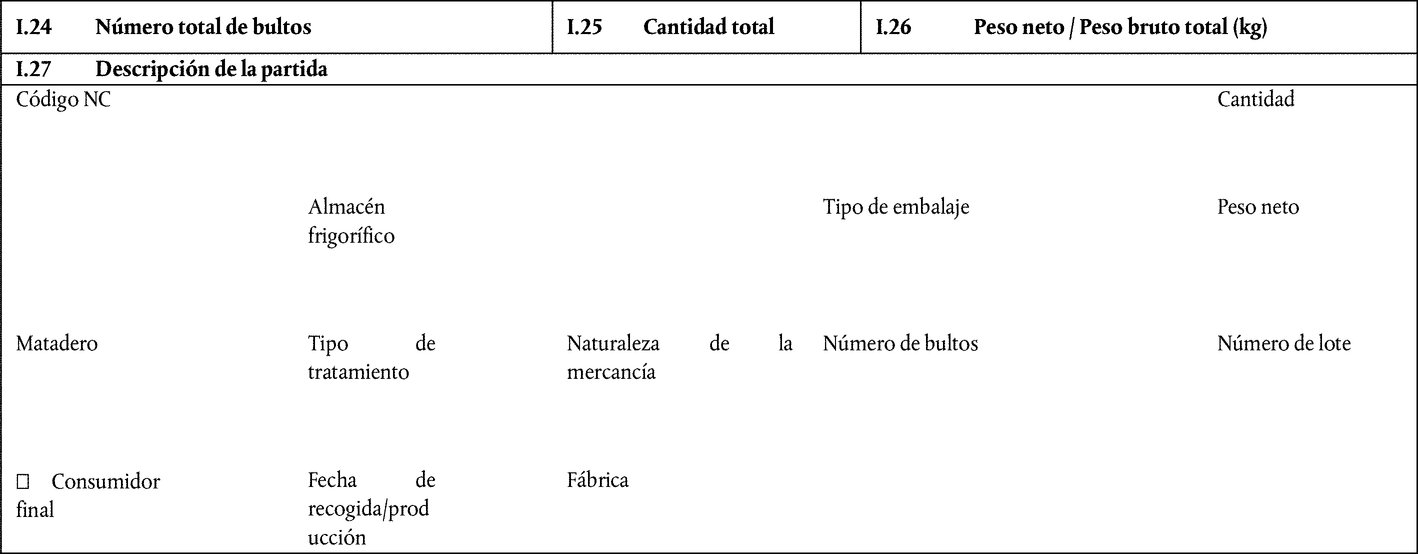            »
»
|
|
18)
|
El capítulo 52 se sustituye por el texto siguiente: « 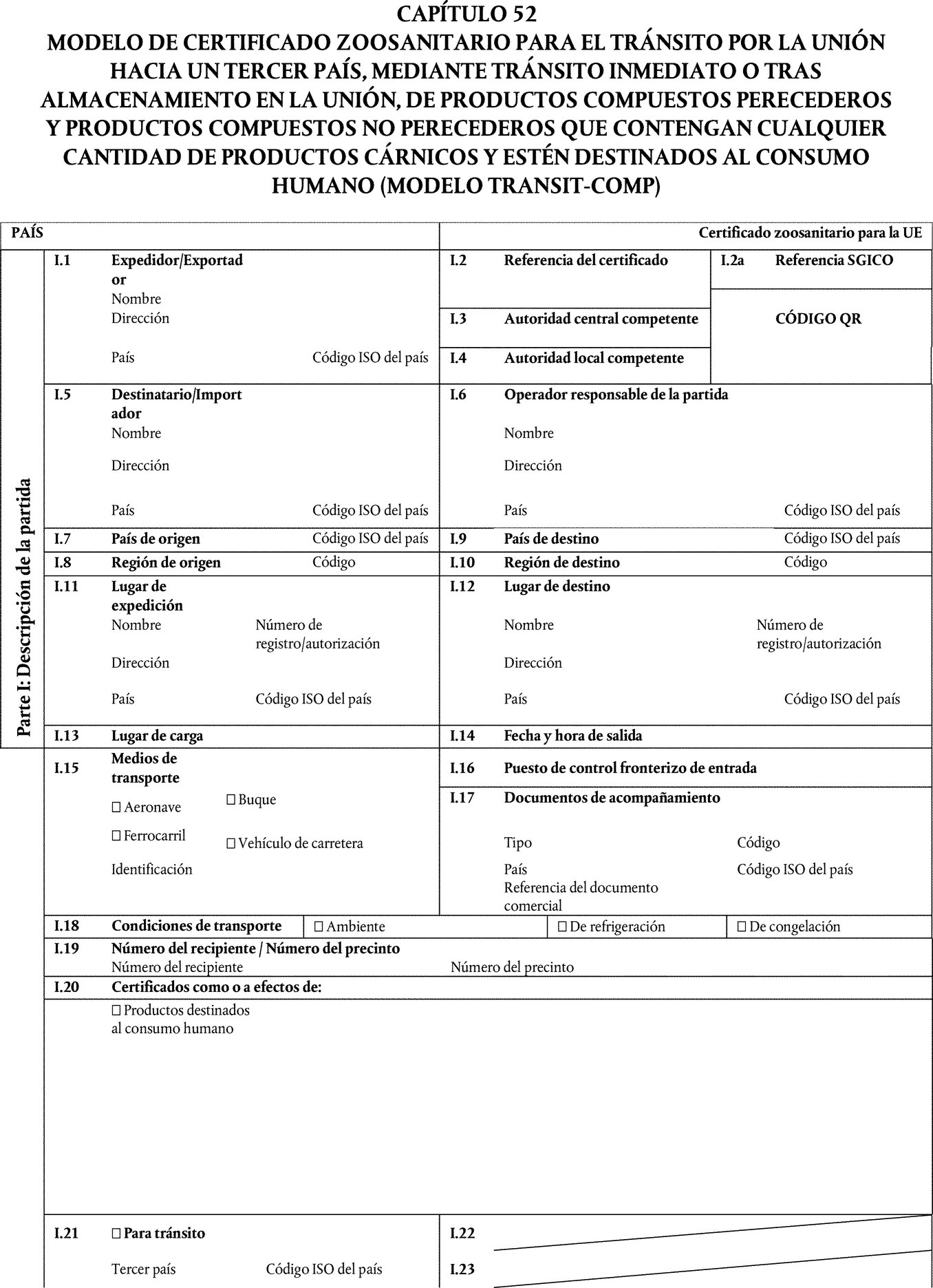 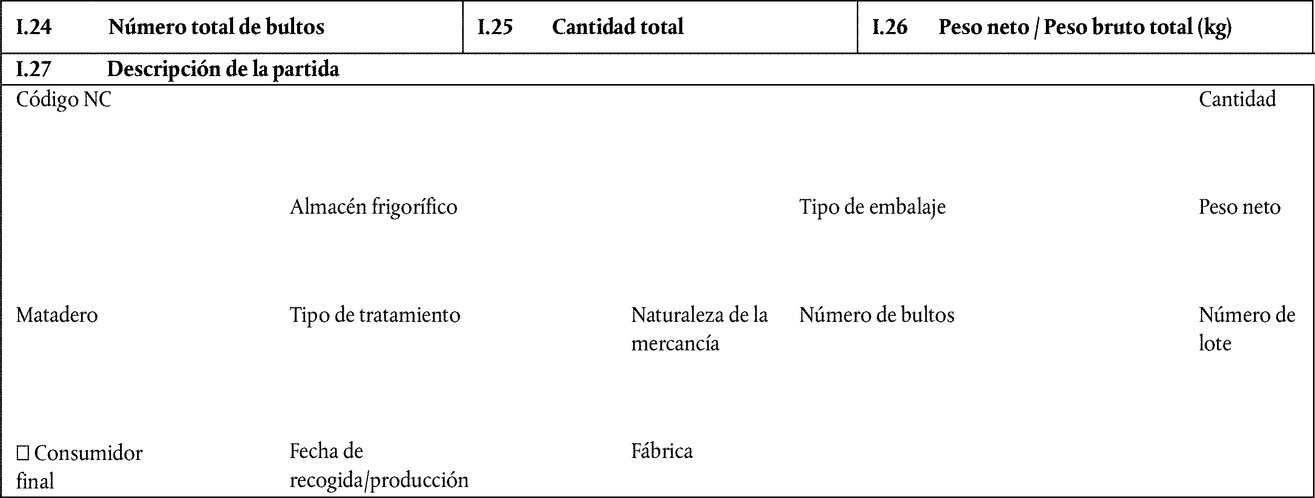       »
»
|
(A) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84).
(B) Reglamento (CE) n.o 1760/2000 del Parlamento Europeo y del Consejo, de 17 de julio de 2000, que establece un sistema de identificación y registro de los animales de la especie bovina y relativo al etiquetado de la carne de vacuno y de los productos a base de carne de vacuno y por el que se deroga el Reglamento (CE) n.o 820/97 del Consejo (DO L 204 de 11.8.2000, p. 1).
(C) https://www.oie.int/es/normas/codigo-terrestre/acceso-en-linea/ »
(D) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84).
(E) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/ »
(F) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84).
(G) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/ »
(H) Reglamento de Ejecución (UE) 2015/1375 de la Comisión, de 10 de agosto de 2015, por el que se establecen normas específicas para los controles oficiales de la presencia de triquinas en la carne (DO L 212 de 11.8.2015, p. 7).»
(I) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84).
(J) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/»
(K) Reglamento Delegado (UE) 2020/692 de la Comisión, de 30 de enero de 2020, que completa el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo en lo referente a las normas para la entrada en la Unión, y para el desplazamiento y la manipulación tras la entrada, de las partidas de determinados animales, productos reproductivos y productos de origen animal (DO L 174 de 3.6.2020, p. 379).
(L) Reglamento Delegado (UE) 2020/689 de la Comisión, de 17 de diciembre de 2019, por el que se completa el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo en lo referente a las normas de vigilancia, los programas de erradicación y el estatus de libre de enfermedad con respecto a determinadas enfermedades de la lista y enfermedades emergentes (DO L 174 de 3.6.2020, p. 211). »
(M) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84).
(N) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/»
(O) Reglamento Delegado (UE) 2020/692 de la Comisión, de 30 de enero de 2020, que completa el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo en lo referente a las normas para la entrada en la Unión, y para el desplazamiento y la manipulación tras la entrada, de las partidas de determinados animales, productos reproductivos y productos de origen animal (DO L 174 de 3.6.2020, p. 379).
(P) Reglamento Delegado (UE) 2020/689 de la Comisión, de 17 de diciembre de 2019, por el que se completa el Reglamento (UE) 2016/429 del Parlamento Europeo y del Consejo en lo referente a las normas de vigilancia, los programas de erradicación y el estatus de libre de enfermedad con respecto a determinadas enfermedades de la lista y enfermedades emergentes (DO L 174 de 3.6.2020, p. 211). »
(Q) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84).
(R) https://www.oie.int/es/normas/codigo-terrestre/acceso-en-linea/»
(S) Reglamento de Ejecución (UE) 2018/1882 de la Comisión, de 3 de diciembre de 2018, relativo a la aplicación de determinadas normas de prevención y control a categorías de enfermedades enumeradas en la lista y por el que se establece una lista de especies y grupos de especies que suponen un riesgo considerable para la propagación de dichas enfermedades de la lista (DO L 308 de 4.12.2018, p. 21). »
(T) Reglamento de Ejecución (UE) 2018/1882 de la Comisión, de 3 de diciembre de 2018, relativo a la aplicación de determinadas normas de prevención y control a categorías de enfermedades enumeradas en la lista y por el que se establece una lista de especies y grupos de especies que suponen un riesgo considerable para la propagación de dichas enfermedades de la lista (DO L 308 de 4.12.2018, p. 21).»
(U) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84).
(V) Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo, de 22 de mayo de 2001, por el que se establecen disposiciones para la prevención, el control y la erradicación de determinadas encefalopatías espongiformes transmisibles (DO L 147 de 31.5.2001, p. 1).
(W) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/»
(X) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84).
(Y) Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo, de 22 de mayo de 2001, por el que se establecen disposiciones para la prevención, el control y la erradicación de determinadas encefalopatías espongiformes transmisibles (DO L 147 de 31.5.2001, p. 1).
(Z) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/»
(AA) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84).
(BB) https://www.oie.int/en/standard-setting/terrestrial-code/access-online/»
(CC) Decisión 2007/453/CE de la Comisión, de 29 de junio de 2007, por la que se establece la situación de los Estados miembros, de terceros países o de regiones de los mismos con respecto a la EEB en función del riesgo de EEB que presentan (DO L 172 de 30.6.2007, p. 84).
(DD) Reglamento (CE) n.o 999/2001 del Parlamento Europeo y del Consejo, de 22 de mayo de 2001, por el que se establecen disposiciones para la prevención, el control y la erradicación de determinadas encefalopatías espongiformes transmisibles (DO L 147 de 31.5.2001, p. 1).
(EE) https://www.oie.int/en/standard-setting/terrestrial-code/access-online»»
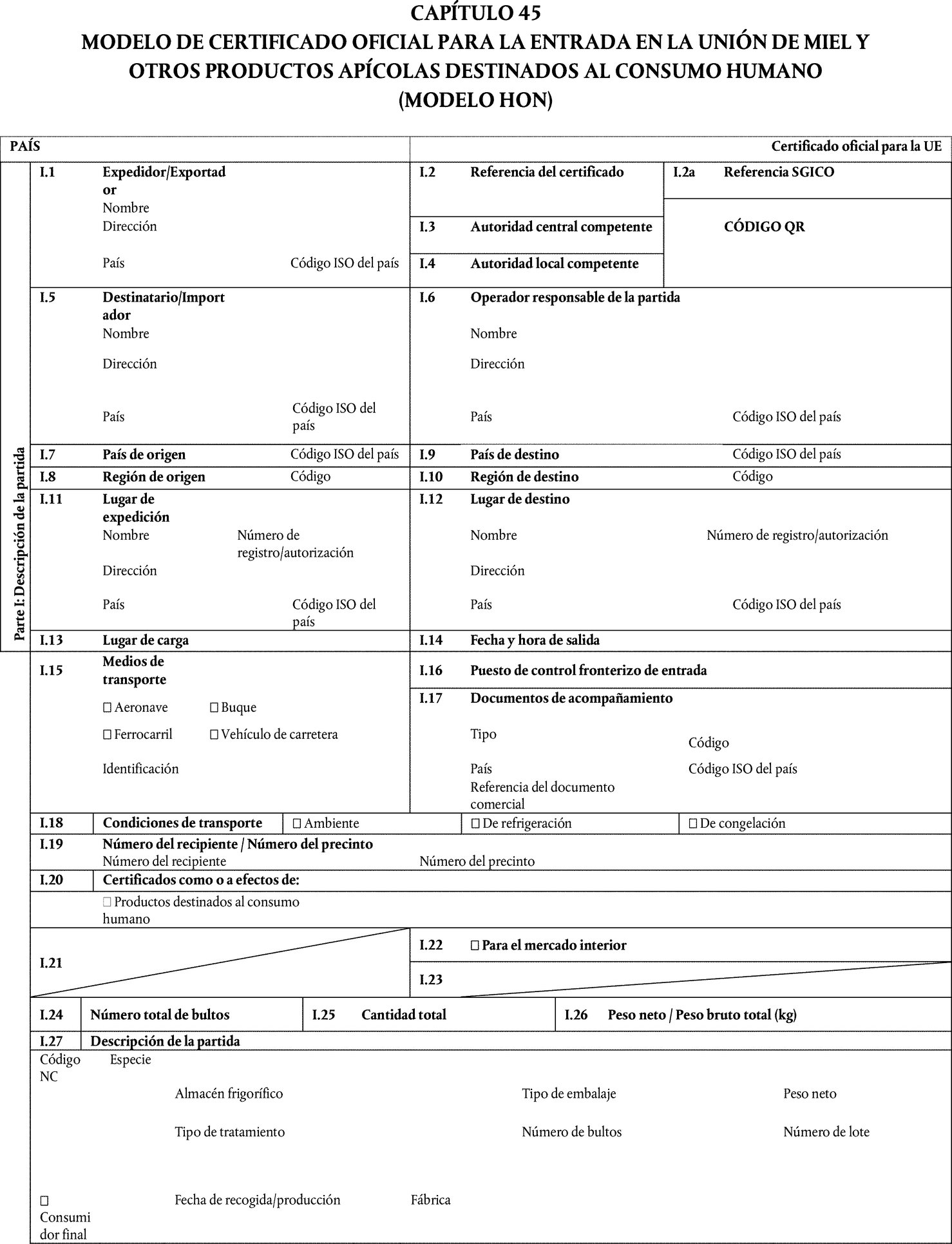

 »;
»;












 »
»







 »
»